Abstract
Hip resurfacing arthroplasty is a concept of hip replacement surgery developed specifically for young and active patients. Femoral bone stock preservation and restoring of normal anatomy of the hip joint allow for better functioning, with increased frequency and duration of sporting activities. Patient-related factors leading to worse outcomes have also been identified. Moreover, concerns about metal-on-metal bearings with adverse reaction to metal debris have led to a recent drop-off in this kind of procedure. The purpose of this study was to evaluate current trends about hip resurfacing and comparing it to standard hip replacement arthroplasty. Hip resurfacing still represents a viable option with a correct indication, in the right hands and using a device with a long track record.
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Introduzione
La protesi di rivestimento dell’anca (HRA), o resurfacing, rappresenta una tecnica chirurgica mirata al trattamento dell’artrosi con una resezione solo parziale della testa femorale (Fig. 1). In considerazione del risparmio osseo permesso da questo intervento e dal ripristino più fisiologico della biomeccanica dell’anca, questa soluzione è stata sviluppata in particolare per i pazienti giovani e attivi.
La HRA è certamente affascinante dal punto di vista concettuale, ma ancora al centro di dibattiti e controversie. Le prime due generazioni dell’HRA che combinavano l’uso di due componenti congruenti nacquero intorno al 1970 diventando uno degli interventi più popolari in Europa e negli Stati Uniti [1]. Denominate Double Cup Arthroplasties, si caratterizzavano per una componente metallica femorale e una acetabolare in polietilene, entrambe cementate [2].
La frammentazione del cemento e l’usura della componente in polietilene portarono la prima generazione di protesi di rivestimento a un rapido declino associato a scarsi risultati nel breve-medio termine e l’abbandono negli anni ’80 [2,3,4]. In seguito, venne dimostrato che le teste femorali di grandi dimensioni che si articolavano con il polietilene causavano osteolisi e debris dell’inserto, generando mobilizzazione protesica precoce [5]. Lo sviluppo del concetto di Metallo-Metallo (MoM) come accoppiamento articolare con un miglioramento della lubrificazione ha donato nuova linfa al concetto di resurfacing.
Intorno agli anni ’90, McMinn e Wagner svilupparono un nuovo sistema in lega Cromo-Cobalto (CrCo) con un cotile press-fit rivestito in idrossiapatite e una cupola cementata. In questo modo si potevano eliminare i problemi dati dall’osteolisi e garantire i vantaggi del risparmio osseo. I risultati a breve termine di questi interventi erano molto promettenti con fratture del collo femorale e mobilizzazione femorale come principale causa di fallimento, rispettivamente nel 5,6 e 2,3% dei casi. Tuttavia, intorno ai primi anni 2000, vennero riportate una serie di sequele tra cui reazioni avverse tissutali (pseudotumors), vasculiti asettiche e metallosi [6]. Nel 2010 due device protesici vennero tolti dal mercato: l’Articular Surface Replacement (ASR, De Puy, Warsaw, IN, USA) per scarsi risultati nel breve termine, a causa del suo design acetabolare, e la Durom Acetabular Component (Zimmer Inc. Warsaw, IN, USA) che venne volontariamente richiamata dalla casa produttrice [7].
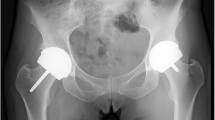
Ad oggi, la Birmingham Hip Resurfacing (BHR, Smith and Nephew, Memphis, TN USA) (Fig. 2) è la protesi di rivestimento maggiormente utilizzata, impiantata per la prima volta nel 1997 in Inghilterra e approvata dalla FDA dieci anni più tardi. Nonostante la sopravvivenza a 10 anni con tassi che variano dall’88 al 99% è ancora da chiarire il suo ruolo esatto nel panorama degli interventi protesici [8].
Vantaggi e svantaggi
Rispetto alla protesi totale di anca, i principali vantaggi della protesi di rivestimento sono: il maggior risparmio osseo femorale prossimale, il ritorno alle attività di impatto dopo 6 mesi dall’intervento [9], una ridotta percentuale di lussazione, il mantenimento della normale anatomia e una semplice chirurgia di revisione. Tuttavia, non sono esenti da svantaggi, tra cui: fallimento precoce con specifici design protesici, fratture del collo femorale, reazioni avverse tissutali (ALTR) e metallosi reattiva [10,11,12,13]. Possiamo vedere un riassunto in Tabella 1.
Selezione del paziente
La selezione del paziente è la chiave per un buon risultato. Le principali indicazioni per HRA sono: il sesso maschile, l’età inferiore a 60 anni e il soggetto attivo con taglia protesica femorale di grandi dimensioni. Diversi autori hanno dimostrato eccellenti risultati in questo tipo di popolazione, con range di sopravvivenza che variano dal 98% a 5 anni fino a 95% a 10 anni. Sono stati però dimostrati diversi fattori che possono aumentare la percentuale di fallimento del HRA e tra questi menzioniamo: l’angolo di inclinazione acetabolare, le taglie femorali di piccole dimensioni, alcuni design protesici, la presenza di un’anca displasica, il sesso femminile, l’età maggiore di 60 anni e la scarsa qualità dell’osso. Il sesso femminile è un fattore di rischio indipendente per fallimento precoce per diversi motivi.
Haughom e collaboratori [14] sottolineano la sua stretta correlazione con le taglie femorali di piccole dimensioni, la maggior prevalenza femminile di anca displasica, la scarsa qualità dell’osso e la maggiore lassità legamentosa. Liu e colleghi [15] hanno dimostrato l’esistenza di una safe zone per il posizionamento acetabolare nel HRA (Relative Acetabular Inclination Limit, RAIL) basato sulla grandezza dell’impianto e sull’angolo di inclinazione acetabolare (AIA). Quando l’AIA scende al di sotto della RAIL diminuiscono considerevolmente i fenomeni di lussazione o di usura. Il sesso femminile è associato ad una AIA aumentata e, quindi, a un maggior rischio di malposizionamento dell’impianto [16,17,18]. La displasia dell’anca è anch’essa un fattore di rischio indipendente. Gross et al [19], analizzando 1.216 HRA, hanno mostrato un tasso di sopravvivenza a 8 anni dei pazienti con DDH del 75%, comparato al 93% per il gruppo di controllo. Inoltre, l’antiversione naturale dell’anca displastica causa una scarsa copertura a livello della porzione anterosuperiore della coppa acetabolare, portando molti chirurghi ad aumentare l’angolo di abduzione (\(>40^{\circ}\)) e, quindi, a un’aumentata usura e a un fallimento precoce. Infine, la maggiore antiversione femorale classica dell’anca displasica aumenta il rischio di edge loading e di potenziale fallimento [20, 21].
Tecnica chirurgica
L’HRA è tecnicamente più complessa di una protesi totale di anca. Numerosi dettagli di tecnica e posizionamento dell’impianto possono influenzare in maniera determinante il risultato dell’intervento. Molte case series hanno dimostrato che esperienza e maggior numero di casi garantiscono migliori risultati e una diminuzione delle complicanze [22,23,24,25]. Il corretto posizionamento della componente acetabolare (inclinazione e antiversione) è di fondamentale importanza per evitare una precoce mobilizzazione delle componenti e il rilascio di ioni metallo. Amstutz e collaboratori [18] hanno introdotto il concetto di Contact patch to rim distance (CPRD, distanza tra il centro di contatto tra il femore e l’acetabolo e il bordo acetabolare), sottolineando che un valore \(<10~\mbox{mm}\) è correlato a un rischio 37 volte maggiore di avere valori elevati di Cobalto ematico e circa 11 volte maggiore di Cromo. Di conseguenza, componenti acetabolari con con un AIA aumentato (\(>55^{\circ}\)) presentano a loro volta un CPRD ridotto, strettamente correlato a fenomeni di precoce usura, metallosi e edge loading. Amstutz conclude che il corretto posizionamento acetabolare debba essere raggiunto con un angolo di abduzione di \(42^{\circ}\pm 10^{\circ}\) e un angolo di antiversione di circa \(15^{\circ}\pm 10^{\circ}\).
La preparazione della componente femorale è di grande importanza per evitare di incorrere in fratture del collo femorale. Un posizionamento varo della componente, associato a un sottile spessore della corticale o a un notching, possono portare a complicanze potenzialmente devastanti che inducono il chirurgo a riporre grande attenzione durante la preparazione femorale [26]. Inoltre, diversi studi sottolineano che teste femorali di piccole dimensione (38–44 mm) sono associate a un aumentato rischio di fallimento a breve termine e a usura [27, 28]. Uno studio biomeccanico di Matharu e colleghi [29] ha dimostrato che componenti femorali di grandi dimensioni promuovono una migliore lubrificazione articolare riducendo, quindi, il rischio di usura.
Riguardo l’approccio chirurgico di prima scelta non esiste un reale consenso. L’approccio più comunemente utilizzato è quello postero-laterale che consente un’eccellente visualizzazione. Nonostante ciò, viene criticato per una possibile compromissione della vascolarizzazione della testa femorale, poiché pone il rischio di violare una delle branche profonde dell’arteria circonflessa mediale, causando aumentato rischio di osteonecrosi. Contrariamente all’approccio posteriore, la via laterale diretta e quella anteriore consentono di preservare le strutture vascolari della testa femorale, anche se nell’approccio anteriore diretto sono riportati un aumentato rischio di frattura e una neuroprassia del nervo femoro-cutaneo laterale.
Uno studio canadese ha valutato 550 casi di HRA senza rilevare una differenza statisticamente significativa tra i tre diversi approcci (anteriore, laterale, posteriore) [30]. Nonostante sia ampiamente diffuso l’utilizzo di impianti ibridi (componente femorale cementata e coppa acetabolare press fit non cementata), ultimamente sono state introdotte soluzioni protesiche senza l’uso del cemento (cementless). Amstutz e collaboratori [31], in un recente studio, hanno voluto confrontare le due diverse tecniche, mostrando che non esiste alcuna differenza statisticamente significativa in termini di outcome clinico, percentuali di fallimento e segni di mobilizzazione radiografica. Gli stessi risultati sono stati ottenuti anche da Tice et al. [32]. Tuttavia, alcuni autori ritengono che questa tecnica sia particolarmente adatta ai pazienti giovani, con una buona qualità dell’osso e che ambiscono a tornare a livelli di sport elevato.
Complicanze
La complicanza più frequente di fallimento precoce nelle HRA è la frattura del collo del femore, responsabile di più del 35% di tutte le revisioni con un’incidenza media del 1,69% [21]. Ovviamente età avanzata, scarsa densità ossea, piccola testa femorale e femoral notching sono associati a un aumentato rischio di frattura [33]. La mobilizzazione delle componenti, soprattutto quella femorale, è un’altra comune causa di fallimento, anche se, come riportato precedentemente, recenti studi sottolineano che uno scorretto posizionamento della componente acetabolare può causare usura e mobilizzazione precoce. Per ovviare all’allentamento della componente femorale il chirurgo deve riporre massima attenzione a fresare correttamente la testa, rimuovendo tutto il materiale cistico o necrotico, oltre ad asciugare attentamente l’osso prima della cementazione e a ottimizzare al massimo l’area di interfaccia osso-cemento con l’esecuzione di piccoli fori ossei [25]. Alcuni autori suggeriscono che un danno vascolare della testa femorale sia il principale responsabile delle fratture, delle mobilizzazioni asettiche e del neck narrowing [34,35,36]: per questo motivo, è molto importante preservare la vascolarità del femore per prevenire complicanze.
Metallurgia
La metallurgia delle componenti protesiche è differente per ogni impianto e altamente influenzata dal processo produttivo. Senza entrare nel dettaglio tecnico, quello che cambia è il contenuto di carburo nella lega metallica e questo particolare influenza la resistenza e il rilascio di ioni [37]. Un alto contenuto di carbonio è associato a un minor tasso di rilascio di ioni [38]. La risposta biologica al rilascio di ioni può essere divisa in reazione: cellulare, locale e sistemica. Il legame diretto del Cr al DNA cellulare è ben documentato [39] e inibisce la riparazione di DNA aberrante. Inoltre, gli ioni metallici possono provocare la formazione di radicali liberi che reagiscono con il DNA indicendo danni alle basi di purina e pirimidina o indurre cross-linking [40]. Modificazioni permanenti del materiale genetico possono rappresentare il primo step nella mutagenesi e carcinogenesi. Al momento attuale non esistono evidenze che la HRA possa causare un rischio aumentato di patologie oncologiche. Sono stati descritti però diversi eventi avversi locali: necrosi estesa [41, 42], osteolisi periprotesica [43, 44] e masse di tessuti molli o pseudotumor [45,46,47]. La causa esatta di questa risposta biologica rimane poco chiara, ma sicuramente alla base rimane una risposta cellulare aberrante al rilascio di ioni metallici [24, 48,49,50,51], senza dimenticare la risposta immunitaria tardiva data da ipersensibilità ritardata [52].
Sembra che ci sia una sostanziale differenza tra le reazioni collegate a un alto tasso di usura (spesso dovuto a malposizionamento) e quelle da ipersensibilità al metallo [50, 53]. La formazione di pseudotumor solidi, semisolidi o liquidi caratterizzati da estesa necrosi, presenza di cellule B, linfociti T e plasmacellule possono essere dovuti alla presenza di debris delle componenti in metallo [54, 55], ma sono stati descritti anche in casi dove l’usura o l’ipersensibilità ritardata non sembravano dei fattori scatenanti [56, 57]. Le protesi BHR e Conserve Plus rimangono ad oggi gli impianti maggiormente utilizzati e studiati con sopravvivenza a 10 anni approssimativamente intorno al 95% [58]. Tuttavia, permangono complicanze legate alla formazione di pseudotumors asintomatici e di metallosi nel lungo e medio periodo, anche se in misura decisamente inferiore rispetto ad altri design ora ritirati dal mercato.
Non esiste consenso sulla sorveglianza postoperatoria del paziente operato di HRA. Si è stabilito che la soglia di normalità dei livelli ematici di CrCo debba essere \(<7~\mbox{ug/L}\) e che tutti i pazienti asintomatici ma con fattori di rischio (DDH, testa femorale piccola, sesso femminile, ridotto CPRD) debbano essere sottoposti a un controllo periodico di tali valori ematici. Si è notato soprattutto che livelli ematici di Co \(>20~\mbox{ug/L}\) sono frequentemente associati ad adverse local tissue reaction (ALTR). Una diagnosi precoce di ALTR consente di intervenire preventivamente sull’impianto, evitando di danneggiare i tessuti molli periprotesici.
Una percentuale maggiore di riassorbimento periprotesico è stata riscontrata nei pazienti positivi ai test cutanei per il cobalto [48, 59], indicando una possibile ipersensibilità ritardata ai metalli, anche se un consenso sulla correlazione tra test cutanei e ipersensibilità organica è lontano dall’essere raggiunto. Sia la risonanza magnetica nucleare (RMN) che l’ecografia sono molto sensibili e specifici per individuare gli pseudotumors nei pazienti con HRA. Ancora non è chiaro quando e se intervenire in caso di presenza di ALTR. Van der Weegan e collaboratori [60] hanno proposto una linea guida di gestione postoperatoria che prevede l’intervento chirurgico di revisione in tutti i pazienti sintomatici con elevati livelli ematici di CrCo associati a pseudotumor di grossi dimensioni, mentre è consigliato l’approccio conservativo nei casi asintomatici con livelli ematici normali di CrCo con neoformazioni di piccole-medie dimensioni.
Discussione e analisi della letteratura
La protesi di rivestimento, come dimostrato da diversi autori [21, 29, 61], è un intervento che presenta un range di sopravvivenza che varia dal 98% a 5 anni al 95% a 10 anni. Questi dati sono da ritenersi validi solo in un paziente selezionato e solamente se eseguiti da un chirurgo esperto con una congrua conoscenza dell’impianto protesico. Matharu e colleghi [29] hanno analizzato 447 HRA con 14 anni di follow-up, riportando una sopravvivenza media del 94,1%. Daniel et al. [21] hanno mostrato una sopravvivenza lievemente maggiore (95,1%), ma con un numero maggiore di pazienti (1.000) e con un follow-up a 15 anni. Entrambi questi studi sono stati condotti da due chirurghi/designer esperti che hanno contribuito a sviluppare il modello protesico. Risultati lievemente inferiori sono stati riportati da diversi autori/non designer [8, 62, 63], confermando il fatto che l’accuratezza della tecnica chirurgica, insieme all’esperienza del primo operatore, sono uno dei principali fattori che influenzano la buona riuscita dell’intervento chirurgico.
Un altro importante fattore da tenere in considerazione è il livello di attività postoperatorio. In alcuni studi, la letteratura ci mostra un livello di attività e qualità di vita superiore per quanto riguarda il resurfacing rispetto alla protesi totale di anca (PTA) [64, 65] e che i pazienti portatori di HRA partecipano più di frequente a sport con tempi di esercizio più lunghi [64, 66]. Allo stesso tempo, però, Banerjee e colleghi [66] ci mostrano diversi fastidi riportati dai pazienti, tra cui: dolore (5,9%), paura (4,6%), diminuzione di forza e resistenza (5,9%) e limitata articolarità (5,3%). In una recente review, Eethakota e collaboratori [67] hanno dimostrato come le protesi di rivestimento abbiano tuttora un tasso di revisione lievemente maggiore rapportato alle PTA per lo stesso gruppo di età. Esistono, però, scarsi studi sul tasso di sopravvivenza a lungo termine delle moderne HRA.
Analizzando il registro australiano (https://aoanjrr.dmac.adelaide.edu.au/en/annual-reports-2013) vengono riportate 266.645 PTA primarie, con un tasso di revisione a 10 anni del 6,6% (95% CI: 6,4–6,8) e dell’8,8% (95% CI: 7,9–9,0) per i pazienti con meno di 55 anni. Il tasso di revisione delle HRA invece era del 7,1% per le componenti inferiori ai 48 mm e 5,9% (95% CI: 5,2–6,6%) per quelle superiori o uguali a 48 mm, sottolineando l’importanza delle dimensioni, ma anche mostrando dei tassi di revisione paragonabili alle PTA.
In generale, dall’analisi dei registri mondiali, appare che il tasso di sopravvivenza sia direttamente collegato a: dimensione dell’impianto, sesso, età e tipo di device utilizzato. Smith et al. [68] hanno evidenziato un tasso di revisione due volte maggiore rispetto alle classiche PTA, supportato dalla meta-analisi sistematica di Marshal e colleghi [69], che ha mostrato un tasso di revisione per le HRA maggiore e presente già nel breve periodo postoperatorio. Altri autori hanno dimostrato che esiste una grossa associazione tra il tipo di protesi utilizzato e il tasso di revisione, sottolineando il fatto che tra i principali fattori di rischio per un fallimento precoce dell’impianto ci siano il design e la geometria protesica [70, 71]. I tassi di complicanza delle HRA sono lievemente inferiori rispetto alle PTA. Eethakota et al. [67] hanno mostrato che nella maggior parte degli studi analizzati ci sia una predominanza di complicanze per le PTA con una maggior prevalenza per le infezioni (profonde e superficiali), la mobilizzazione asettica, la metallosi e le fratture periprotesiche. Infine, il tasso di lussazione è risultato essere maggiore nelle PTA, sottolineando il fatto che uno dei principali vantaggi delle HRA sia la capacità di essere poco invasivi, mantenendo la normale biomeccanica articolare [67].
Ad oggi risulta difficile stabilire la superiorità di una tecnica rispetto a un’altra, poiché non esistono ancora studi a lungo termine sugli impianti protesici HRA di nuova generazione. Una prospettiva futura è rappresentata dal resurfacing ceramica-ceramica che, al momento attuale, è in fase di test clinico in pochi centri ed è formata da due componenti press-fit totalmente in ceramica con uno strato di idrossiapatite a diretto contatto con la ceramica per favorire l’osteointegrazione, ma nessun metal-back. Questo device potrebbe sicuramente eliminare il problema del metallo-metallo, ma adesso non possiamo ancora capire se non possa portare altre complicanze come lo squeaking o le rotture della ceramica.
Conclusioni
L’analisi della letteratura attuale non ci permette di trarre delle conclusioni chiare e univoche sull’utilizzo dell’HRA. Gli studi ci dimostrano che in mani esperte e con un’indicazione corretta può rappresentare un’ottima soluzione per garantire al paziente giovane e sportivo un impianto più funzionale rispetto alla tradizione protesi totale di anca. Sicuramente rappresenta un intervento con una lunga curva di apprendimento e che necessita di un numero di impianti annuale elevato per garantire dei buoni risultati. Quindi il paziente di sesso maschile, giovane, sportivo, non displasico, con dimensioni del femore sopra i 48 mm che incontra un chirurgo esperto e che usa la BHR potrebbe avere delle ottime possibilità di ottenere un impianto altamente funzionale e durevole. Ovviamente, perché un chirurgo possa trovare annualmente un buon numero di pazienti con tutte queste caratteristiche insieme, deve lavorare in un centro ad alta specializzazione e con volumi elevati. La HRA, rimanendo un’opzione interessante, richiede progressi di tecniche e materiali per trovare più spazio nella pratica quotidiana.
Bibliografia
Amstutz HC, Le Duff MJ (2006) Background of metal-on-metal resurfacing. Proc Inst Mech Eng H 220(2):85–94
Amstutz HC, Dorey F, O’Carroll PF (1986) THARIES resurfacing arthroplasty. Evolution and long-term results. Clin Orthop Relat Res 213:92–114
Howie DW, Campbell D, McGee M, Cornish BL (1990) Wagner resurfacing hip arthroplasty. The results of one hundred consecutive arthroplasties after eight to ten years. J Bone Jt Surg, Am 72(5):708–714
Schmalzried TP, Guttmann D, Grecula M, Amstutz HC (1994) The relationship between the design, position, and articular wear of acetabular components inserted without cement and the development of pelvic osteolysis. J Bone Jt Surg, Am 76(5):677–688
Kabo JM, Gebhard JS, Loren G, Amstutz HC (1993) In vivo wear of polyethylene acetabular components. J Bone Jt Surg, Br 75(2):254–258
Grammatopolous G, Pandit H, Kwon YM et al. (2009) Hip resurfacings revised for inflammatory pseudotumour have a poor outcome. J Bone Jt Surg, Br 91(8):1019–1024
Jameson SS, Baker PN, Mason J et al. (2012) Independent predictors of revision following metal-on-metal hip resurfacing: a retrospective cohort study using National Joint Registry data. J Bone Jt Surg, Br 94(6):746–754
Mehra A, Berryman F, Matharu GS et al. (2015) Birmingham hip resurfacing: a single surgeon series reported at a minimum of 10 years follow-up. J Arthroplast 30(7):1160–1166
Bedigrew KM, Ruh EL, Zhang Q et al. (2012) 2011 Marshall Urist Young Investigator Award: when to release patients to high-impact activities after hip resurfacing. Clin Orthop Relat Res 470(1):299–306
Gross TP, Liu F (2014) Current status of modern fully porous coated metal-on-metal hip resurfacing arthroplasty. J Arthroplast 29(1):181–185
Ribas M, Cardenas C, Astarita E et al. (2014) Hip resurfacing arthroplasty: mid-term results in 486 cases and current indication in our institution. Hip Int 24(Suppl 10):S19–24
Robinson PG, Wilkinson AJ, Meek RM (2014) Metal ion levels and revision rates in metal-on-metal hip resurfacing arthroplasty: a comparative study. Hip Int 24(2):123–128
Johnson AJ, Le Duff MJ, Yoon JP et al. (2013) Metal ion levels in total hip arthroplasty versus hip resurfacing. J Arthroplast 28(7):1235–1237
Haughom BD, Erickson BJ, Hellman MD, Jacobs JJ (2015) Do complication rates differ by gender after metal-on-metal hip resurfacing arthroplasty? A systematic review. Clin Orthop Relat Res 473(8):2521–2529
Liu F, Gross TP (2013) A safe zone for acetabular component position in metal-on-metal hip resurfacing arthroplasty: winner of the 2012 HAP PAUL award. J Arthroplast 28(7):1224–1230
Rahman WA, Greidanus NV, Siegmeth A et al. (2013) Patients report improvement in quality of life and satisfaction after hip resurfacing arthroplasty. Clin Orthop Relat Res 471(2):444–453
Al-Hamad M, Le Duff MJ, Takamura KM, Amstutz HC (2014) Acetabular component thickness does not affect mid-term clinical results in hip resurfacing. Clin Orthop Relat Res 472(5):1528–1534
Amstutz HC, Le Duff MJ, Johnson AJ (2012) Socket position determines hip resurfacing 10-year survivorship. Clin Orthop Relat Res 470(11):3127–3133
Gross TP, Liu F (2012) Prevalence of dysplasia as the source of worse outcome in young female patients after hip resurfacing arthroplasty. Int Orthop 36(1):27–34
Amstutz HC, Le Duff MJ (2015) Aseptic loosening of cobalt chromium monoblock sockets after hip resurfacing. Hip Int 25(5):466–470
Daniel J, Pradhan C, Ziaee H et al. (2014) Results of Birmingham hip resurfacing at 12 to 15 years: a single-surgeon series. Bone Jt J 96-b(10):1298–1306
Mont MA, Marker DR, Smith JM et al. (2009) Resurfacing is comparable to total hip arthroplasty at short-term follow-up. Clin Orthop Relat Res 467(1):66–71
Marker DR, Seyler TM, Jinnah RH et al. (2007) Femoral neck fractures after metal-on-metal total hip resurfacing: a prospective cohort study. J Arthroplast 22(7 Suppl 3):66–71
Siebel T, Maubach S, Morlock MM (2006) Lessons learned from early clinical experience and results of 300 ASR hip resurfacing implantations. Proc Inst Mech Eng H 220(2):345–353
Amstutz HC, Le Duff MJ (2015) Hip resurfacing: history, current status, and future. Hip Int 25(4):330–338
Tai CL, Chen YC, Hsieh PH (2014) The effects of necrotic lesion size and orientation of the femoral component on stress alterations in the proximal femur in hip resurfacing—a finite element simulation. BMC Musculoskelet Disord 15:262
Dowson D, Hardaker C, Flett M, Isaac GH (2004) A hip joint simulator study of the performance of metal-on-metal joints: part I: the role of materials. J Arthroplast 19(8 Suppl 3):118–123
Canadian Arthroplasty Society (2013) The Canadian Arthroplasty Society’s experience with hip resurfacing arthroplasty. An analysis of 2773 hips. Bone Jt J 95-b(8):1045–1051
Matharu GS, Berryman F, Brash L et al. (2015) Predicting high blood metal ion concentrations following hip resurfacing. Hip Int 25(6):510–519
Zylberberg AD, Nishiwaki T, Kim PR, Beaule PE (2015) Clinical results of the conserve plus metal on metal hip resurfacing: an independent series. J Arthroplast 30(1):68–73
Amstutz HC, Le Duff MJ (2018) Is a cementless fixation of the femoral component suitable for metal-on-metal hip resurfacing arthroplasty? Hip Int. https://doi.org/10.1177/1120700018815055
Tice A, Kim P, Dinh L et al. (2015) A randomised controlled trial of cemented and cementless femoral components for metal-on-metal hip resurfacing: a bone mineral density study. Bone Jt J 97-b(12):1608–1614
Davis ET, Olsen M, Zdero R et al. (2013) Predictors of femoral neck fracture following hip resurfacing: a cadaveric study. J Arthroplast 28(1):110–116
Shimmin AJ, Back D (2005) Femoral neck fractures following Birmingham hip resurfacing: a national review of 50 cases. J Bone Jt Surg, Br 87(4):463–464
Beaule PE, Campbell P, Lu Z et al. (2006) Vascularity of the arthritic femoral head and hip resurfacing. J Bone Jt Surg, Am 88(Suppl 4):85–96
Zustin J, Krause M, Breer S et al. (2010) Morphologic analysis of periprosthetic fractures after hip resurfacing arthroplasty. J Bone Jt Surg, Am 92(2):404–410
Catelas I, Bobyn JD, Medley JB et al. (2003) Size, shape, and composition of wear particles from metal-metal hip simulator testing: effects of alloy and number of loading cycles. J Biomed Mater Res, Part A 67(1):312–327
Vendittoli PA, Lavigne M, Girard J, Roy AG (2006) A randomised study comparing resection of acetabular bone at resurfacing and total hip replacement. J Bone Jt Surg, Br 88(8):997–1002
Wolf T, Kasemann R, Ottenwalder H (1989) Molecular interaction of different chromium species with nucleotides and nucleic acids. Carcinogenesis 10(4):655–659
Dizdaroglu M, Jaruga P, Birincioglu M, Rodriguez H (2002) Free radical-induced damage to DNA: mechanisms and measurement. Free Radic Biol Med 32(11):1102–1115
Boardman DR, Middleton FR, Kavanagh TG (2006) A benign psoas mass following metal-on-metal resurfacing of the hip. J Bone Jt Surg, Br 88(3):402–404
Ollivere B, Darrah C, Barker T et al. (2009) Early clinical failure of the Birmingham metal-on-metal hip resurfacing is associated with metallosis and soft-tissue necrosis. J Bone Jt Surg, Br 91(8):1025–1030
Amstutz HC, Wisk LE, Le Duff MJ (2011) Sex as a patient selection criterion for metal-on-metal hip resurfacing arthroplasty. J Arthroplast 26(2):198–208
von Schewelov T, Sanzen L (2010) Catastrophic failure due to aggressive metallosis 4 years after hip resurfacing in a woman in her forties—a case report. Acta Orthop 81(3):402–404
Gruber FW, Bock A, Trattnig S et al. (2007) Cystic lesion of the groin due to metallosis: a rare long-term complication of metal-on-metal total hip arthroplasty. J Arthroplast 22(6):923–927
De Haan R, Campbell PA, Su EP, De Smet KA (2008) Revision of metal-on-metal resurfacing arthroplasty of the hip: the influence of malpositioning of the components. J Bone Jt Surg, Br 90(9):1158–1163
Hart AJ, Sabah S, Henckel J et al. (2009) The painful metal-on-metal hip resurfacing. J Bone Jt Surg, Br 91(6):738–744
Davies AP, Willert HG, Campbell PA et al. (2005) An unusual lymphocytic perivascular infiltration in tissues around contemporary metal-on-metal joint replacements. J Bone Jt Surg, Am 87(1):18–27
Willert HG, Buchhorn GH, Fayyazi A et al. (2005) Metal-on-metal bearings and hypersensitivity in patients with artificial hip joints. A clinical and histomorphological study. J Bone Jt Surg, Am 87(1):28–36
Catelas I, Lehoux EA, Hurda I et al. (2015) Do patients with a failed metal-on-metal hip implant with a pseudotumor present differences in their peripheral blood lymphocyte subpopulations? Clin Orthop Relat Res 473(12):3903–3914
Glyn-Jones S, Pandit H, Kwon YM et al. (2009) Risk factors for inflammatory pseudotumour formation following hip resurfacing. J Bone Jt Surg, Br 91(12):1566–1574
Pandit H, Vlychou M, Whitwell D et al. (2008) Necrotic granulomatous pseudotumours in bilateral resurfacing hip arthoplasties: evidence for a type IV immune response. Virchows Arch 453(5):529–534
Campbell P, Shimmin A, Walter L, Solomon M (2008) Metal sensitivity as a cause of groin pain in metal-on-metal hip resurfacing. J Arthroplast 23(7):1080–1085
Langton DJ, Sidaginamale RP, Joyce TJ et al. (2013) The clinical implications of elevated blood metal ion concentrations in asymptomatic patients with MoM hip resurfacings: a cohort study. BMJ Open 3(3):e001541
Pandit H, Glyn-Jones S, McLardy-Smith P et al. (2008) Pseudotumours associated with metal-on-metal hip resurfacings. J Bone Jt Surg, Br 90(7):847–851
Malviya A, Holland JP (2009) Pseudotumours associated with metal-on-metal hip resurfacing: 10-year Newcastle experience. Acta Orthop Belg 75(4):477–483
Campbell P, Ebramzadeh E, Nelson S et al. (2010) Histological features of pseudotumor-like tissues from metal-on-metal hips. Clin Orthop Relat Res 468(9):2321–2327
Coulter G, Young DA, Dalziel RE, Shimmin AJ (2012) Birmingham hip resurfacing at a mean of ten years: results from an independent centre. J Bone Jt Surg, Br 94(3):315–321
Park YS, Moon YW, Lim SJ et al. (2005) Early osteolysis following second-generation metal-on-metal hip replacement. J Bone Jt Surg, Am 87(7):1515–1521
van der Weegen W, Sijbesma T, Hoekstra HJ et al. (2014) Treatment of pseudotumors after metal-on-metal hip resurfacing based on magnetic resonance imaging, metal ion levels and symptoms. J Arthroplast 29(2):416–421
Moroni A, Miscione MT, Orsini R et al. (2017) Clinical and radiographic outcomes of the Birmingham Hip Resurfacing arthroplasty at a minimum follow-up of 10 years: results from an independent centre. Hip Int 27(2):134–139
Azam MQ, McMahon S, Hawdon G, Sankineani SR (2016) Survivorship and clinical outcome of Birmingham hip resurfacing: a minimum ten years’ follow-up. Int Orthop 40(1):1–7
Holland JP, Langton DJ, Hashmi M (2012) Ten-year clinical, radiological and metal ion analysis of the Birmingham Hip Resurfacing: from a single, non-designer surgeon. J Bone Jt Surg, Br 94(4):471–476
Narvani AA, Tsiridis E, Nwaboku HC, Bajekal RA (2006) Sporting activity following Birmingham hip resurfacing. Int J Sports Med 27(6):505–507
Naal FD, Maffiuletti NA, Munzinger U, Hersche O (2007) Sports after hip resurfacing arthroplasty. Am J Sports Med 35(5):705–711
Banerjee M, Bouillon B, Banerjee C et al. (2010) Sports activity after total hip resurfacing. Am J Sports Med 38(6):1229–1236
Eethakota VV, Vaishnav V, Johnston L (2018) Comparison of revision risks and complication rates between total HIP replacement and HIP resurfacing within the similar age group. Surgeon 16(6):339–349
Smith TO, Nichols R, Donell ST, Hing CB (2010) The clinical and radiological outcomes of hip resurfacing versus total hip arthroplasty: a meta-analysis and systematic review. Acta Orthop 81(6):684–695
Marshall DA, Pykerman K, Werle J et al. (2014) Hip resurfacing versus total hip arthroplasty: a systematic review comparing standardized outcomes. Clin Orthop Relat Res 472(7):2217–2230
Vendittoli PA, Roy A, Mottard S et al. (2010) Metal ion release from bearing wear and corrosion with 28 mm and large-diameter metal-on-metal bearing articulations: a follow-up study. J Bone Jt Surg, Br 92(1):12–19
Garbuz DS, Tanzer M, Greidanus NV et al. (2010) The John Charnley Award: metal-on-metal hip resurfacing versus large-diameter head metal-on-metal total hip arthroplasty: a randomized clinical trial. Clin Orthop Relat Res 468(2):318–325
Author information
Authors and Affiliations
Corresponding author
Ethics declarations
Conflitto di interesse
Gli autori Luca Gala e Filippo Calanna dichiarano di non avere alcun conflitto di interesse.
Consenso informato e conformità agli standard etici
Tutte le procedure descritte nello studio e che hanno coinvolto esseri umani sono state attuate in conformità alle norme etiche stabilite dalla dichiarazione di Helsinki del 1975 e successive modifiche. Il consenso informato è stato ottenuto da tutti i pazienti inclusi nello studio.
Human and Animal Rights
L’articolo non contiene alcuno studio eseguito su esseri umani e animali da parte degli autori.
Rights and permissions
About this article
Cite this article
Calanna, F., Gala, L. Protesi di rivestimento di anca. LO SCALPELLO 33, 116–122 (2019). https://doi.org/10.1007/s11639-019-00310-6
Published:
Issue Date:
DOI: https://doi.org/10.1007/s11639-019-00310-6