Background:
Telomerase activity in a human lymphoblastoid cell line with wild-type p53 status (TK6) was previously shown to be rapidly induced by ionizing radiation doses as low as 10 cGy. Since this low-dose response was absent in a closely related cell line overexpressing a mutant form of p53 (WTK1), the putative involvement of p53 was further investigated using stable human papillomavirus 16 (HPV16) E6 transfectants of these cell lines. The E6 product mediates rapid degradation of wild-type p53, but has also been found to upregulate telomerase.
Material and Methods:
Telomerase activity in HPV16 E6 transfectants of the human lymphoblastoid cell lines TK6 and WTK1 was measured by PCR/ELISA and was quantified using internal standards (titration by cell number) run within each separate assay. Mean telomere length was determined by Southern hybridization of terminal restriction fragments with a biotin-labeled telomeric DNA probe.
Results:
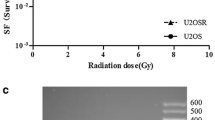
The TK6E6 and the WTK1E6 cells exhibited higher baseline telomerase activities than the parental cells. This was also accompanied by increased telomere lengths. Radiation exposure (up to 10 Gy) was unable to significantly further enhance telomerase activities, although the dynamic range of the assay would have allowed to record higher signals.
Conclusion:
The lacking radiation induction of telomerase activities in the E6 transfectants could reflect saturation, if E6 and radiation would share a common pathway of telomerase upregulation. Present evidence from the literature, however, suggests that E6 mediates telomerase reverse transcriptase (TERT) subunit transcriptional activation, whereas radiation signals to posttranscriptional/posttranslational control of telomerase activity. Therefore, the present data enforce the previous hypothesis of a p53 dependence of telomerase upregulation by low doses of radiation and its abrogation, likely due to p53 degradation, in E6-expressing cells.
Hintergrund:
Eine vorhergehende Studie an humanen Lymphoblasten mit Wildtyp-p53-Status (TK6) zeigte eine rasche Induktion der Telomeraseaktivität bereits durch kleine Strahlendosen (10 cGy). Da dieser Effekt in einer eng verwandten Zelllinie mit mutiertem p53 (WTK1) nicht auftrat, sollte die vermutete Rolle von p53 durch Verwendung der mit HPV16 (humanes Papillomavirus 16) E6 stabil transfizierten Zelllinien weiter untersucht werden. Das E6-Produkt vermittelt die rasche Degradation von p53, ist aber auch als Aktivator der Telomerase bekannt.
Material und Methodik:
Die Telomeraseaktivität in mit HPV16 E6 transfizierten Zelllinien (TK6E6 und WTK1E6) wurde mittels PCR/ELISA gemessen und anhand interner Standards in jedem separaten Assay quantifiziert. Zur Bestimmung der mittleren Telomerlängen diente die Southern-Hybridisierung terminaler Restriktionsfragmente mit einer biotinylierten Telomersonde.
Ergebnisse:
Die TK6E6- und WTK1E6-Zellen zeigten eine gegenüber den parentalen Zellen deutlich erhöhte Telomeraseaktivität und verlängerte Telomere. Bestrahlung (bis 10 Gy) konnte diese Telomeraseaktivität nicht signifikant steigern, obwohl der dynamische Bereich des verwendeten Assays eine Detektion höherer Werte erlaubt hätte.
Schlussfolgerung:
Die fehlende Induktion der Telomeraseaktivität nach Bestrahlung in E6-transfizierten Zellen könnte als ein Sättigungsphänomen interpretiert werden, wenn ein gemeinsamer Pfad der E6- und der strahleninduzierten Regulation der Telomerase unterstellt wird. Dies widerspricht aber aktuellen Ergebnissen aus der Literatur, wonach E6 Transaktivierung der Telomerase-Reverse-Transkriptase-(TERT-)Untereinheit vermittelt, während Bestrahlung die Telomeraseaktivität offenbar über posttranskriptionelle/posttranslationale Mechanismen reguliert. Die vorliegenden Daten unterstreichen daher die frühere Vermutung einer p53-Abhängigkeit der bei kleinen Strahlendosen gemessenen Telomeraseinduktion, die in E6 exprimierenden Zellen, vermutlich durch die p53-Degradation, supprimiert ist.
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
Author information
Authors and Affiliations
Corresponding author
Rights and permissions
About this article
Cite this article
Neuhof, D., Auberger, F., Ruess, A. et al. Abrogation of Radiation-Inducible Telomerase Upregulation in HPV16 E6 Transfectants of Human Lymphoblasts. Strahlenther Onkol 180, 52–56 (2004). https://doi.org/10.1007/s00066-004-1129-1
Received:
Accepted:
Issue Date:
DOI: https://doi.org/10.1007/s00066-004-1129-1