Abstract
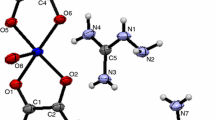
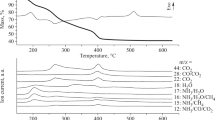
A new molybdenum(VI) complex, Li2[Mo2O6(C2O4)] · 2 H2O (LMO), was prepared and characterized by chemical analysis and IR spectral studies. Its thermal decomposition was studied by using TG and DTA techniques. LMO loses its two moles of water between 75 and 170° to give the anhydrous product, which decomposes in three stages between 240 and 380°. The first two stages occur in the temperature ranges 240–280° and 280–305°, to give intermediates with the tentative compositions Li6[Mo6O19(C2O4)2] and Li6[Mo6O20(C2O4)], respectively. In the third stage, which extends up to 380°, Li6[Mo6O20(C2O4)] decomposes to give the end-product, Li2Mo2O7.
Zusammenfassung
Ein neuer Molybdän(VI)-Komplex der Formel Li2[Mo2O6(C2O4)] · 2 H2O (LMO) wurde dargestellt und durch chemische Analyse und IR-spektroskopisch charakterisiert. Die thermische Zersetzung dieses Komplexes wurde mittels TG und DTA untersucht. LMO verliert die zwei Wassermoleküle zwischen 75 und 170° unter Bildung des wasserfreien Produktes, das zwischen 240 und 380° in drei Stufen zersetzt wird. Die in den Temperaturbereich von 240–280° und 280–305° verlaufenden ersten zwei Reaktionsschritte ergeben Intermediäre der tentativen Zusammensetzung Li6[Mo6O19(C2O4)2] bzw. Li6[Mo6O20(C2O4)]. In dem sich bis 380° erstreckenden dritten Reaktionsschritt wird Li6[Mo6O20(C2O4)] unter Bildung des Endproduktes Li2Mo2O7 zersetzt.
Резюме
Получено новое компл ексное соединение шестивалентного мол ибдена с общей формулой Li2[MO2O6(C2O4] · 2 Н2О и и дентифицированное химическим анализом и ИК спектроскопией. Терм ическое разложение к омплекса изучено методом ТГ и Д ТА. В интер-вале температур 70–170° соедин ение теряет две молек улы воды, образуя безводное соединение, разлагаю щееся в три стадии в ин тервале температур 240–380°. Первы е две стадии протекают в об ласти температур 240–280° и 280–305° с образованием промеж у-точных продуктов состава Li6[Mo6O19(C2O4)2] и Li6[Mo6O20(C2O4)]. Последнее соедине-ни е разлагается на треть ей стадии при темпера туре до 380° с образованием конечн ого продукта Li2Mo2O7.
Article PDF
Similar content being viewed by others
Explore related subjects
Discover the latest articles, news and stories from top researchers in related subjects.Avoid common mistakes on your manuscript.
References
P. C. H. Mitchell, Quart. Rev. Chem. Soc., 20 (1966) 103.
S. P. Goel and P. N. Mehrotra, Thermochim. Acta, 68 (1983) 137.
S. P. Goel and P. N. Mehrotra, Thermochim. Acta, 70 (1983) 201.
K. Nakamoto, Infrared Spectra of Inorganic and Coordination Compounds, John Wiley, New York, 1970, pp. 245.
J. Fujita, A. E. Martel and K. Nakamoto, J. Chem. Phys., 36 (1962) 324.
C. G. Barraclough, J. Lewis and R. S. Nyholm, J. Chem. Soc. (1959) 3552.
W. P. Griffith, J. Chem. Soc., (1963) 5345.
M. Cousins and M. L. H. Green, J. Chem. Soc., (1964) 1567.
V. B. Reddy and P. N. Mehrotra, J. Chem. Tech. Biotechnol., 30 (1980) 504.
V. B. Reddy and P. N. Mehrotra, J. Chinese Chem. Soc., 29 (1982) 119.
T. Dupuis and M. Viltange, Mikrochim. Ichnoanal. Acta, (1963) 232.
J. M. Reau and C. Fouassier, Bull. Soc. Chim. France, 2 (1971) 398.
Author information
Authors and Affiliations
Additional information
The authors are grateful to Prof. S. N. Tandon, Head of the Chemistry Department, for providing the research facilities.
Rights and permissions
About this article
Cite this article
Goel, S.P., Mehrotra, P.N. IR and thermal studies on lithium oxomolybdenum(VI) oxalate. Journal of Thermal Analysis 30, 145–151 (1985). https://doi.org/10.1007/BF02128124
Received:
Revised:
Issue Date:
DOI: https://doi.org/10.1007/BF02128124