Summary
We studied the effect of β-indoleacetic acid (IAA), α-naphthylacetic acid (NAA), kinetin (K), 6-benzylaminopurine (BAP) and gibberellic acid (GA3) on development of isolated meristems of four potato cultivars (subsp. tuberosum). GA3 had a stimulating effect on in vitro meristem growth. The differences among the cultivars are presented. K+IAA+GA3 induced formation of multiple shoots. We describe a method of continual plant multiplication under in vitro conditions and propose the produce for maintenance, multiplication and virus eradication of potato germplasm and cultivars.
Zusammenfassung
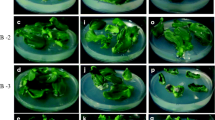
Von vier Kartoffelsorten (Blanik, Cira, Nora und Radka) wurden die Meristemspitzen entnommen. Der Nährboden enthielt Makround Mikroelemente gemäss Murashige & Skoog (1962), Vitamine entsprechend B-5 (Gamborg et al., 1968), 100mg/l Inositol, 30 g/l Saccharose und 8 g/l Agar. Wir untersuchten die Wirkung von β-Indolessigsäure (IAA), α-Naphytlessigsäure (NAA), Kinetin (K), 6-Benzylaminopurin (BAP) und Gibberellinsäure (GA3). Auf den Nährböden mit IAA und NAA wurde mangelhaftes Triebwachstum und unvollständige Blattentwicklung (Abb. 1) festgestellt; die Pflanzen konnten nicht in Erde versetzt werden. K (0.1 μM) induzierte vollständige Pflanzenentwicklung (Tabelle 1), während BAP (0,1μM) die Triebenentwicklung anregte, worauf die Bewurzelung auf Nährboden mit 0,1 μM IAA (Abb. 2) erfolgte. Alle GA3-Konzentrationen hatten einen vorteilhaften Einfluss auf die Entwicklung von Pflänzchen aus Meristemspitzen (Abb. 1 und Tabelle 1). Optimales Wachstum und rasche Entwicklung der Pflanzen aller vier Sorten wurde mit dem Nährboden mit IAA+K+GA3 erreicht. Mehrfache Triebbildung erfolgte auf den Medien mit erhöhten GA3-Konzentrationen (5 und 10 μM), speziell bei den Sorten Cira und Blanik (Abb. 3). Die Pflanzen aus der Meristemspitzenkultur konnten unter sterilen Bedingungen in Perlit, das mit der Hoagland's-Lösung und mit einem Zusatz von 0,1 μM IAA gesättigt war, fortlaufend vermehrt werden. Die Pflanzen entwickeln sich aus Achselknospen. Ein Steckling aus einem Meristem ist fähig, 5–8 Pflanzen in zwei Monaten hervorzubringen. Der Artikel beschreibt das System der mehrfachen Triebbildung und die laufende Fortpflanzung in vitro zur Erhaltung und Vermehrung von Kartoffel-Keimplasma (Westcott et al., 1977) und virusfreien Züchtungen (Abb. 4).
Résumé
Des méristèmes apicaux ont été prélevés sur quatre variétés de pommes de terre: Blanik, Cira, Nora et Radka. Le milieu de culture contenait des macro-et microéléments d'après les indications de Murashige & Skoog (1962), des vitamines B-5 (d'après Gamborg et al., 1968), 100 mg/l d'inositol, 30 g/l de sucrose et 8 g/l d'agar. Nous avons étudié l'action de l'acide β-indoleacetic (IAA), de l'acide α-naphtylacétique (NAA), de la kinétine (K), de la 6-benzylaminopurine (BAP) et de l'acide gibberellic (GA3). Sur les milieux contenant de l'IAA et du NAA, nous avons observé un développement imparfait des pousses, et un développement partiel des feuilles (fig. l); les plantes ne pouvaient pas être transplantées en terre. K (0,1 μM) a induit un développement complet des plantes (tableau 1) tandis que le BAP (0,1 μM) a stimulé le développement des pousses suivi de leur enracinement dans le milieu contenant 0,1 μM d'IAA (fig. 2). Toutes les concentrations de GA3 ont eu un effet bénéfique sur le développement des plantules issues de méristèmes apicaux (fig. 1 et tableau 1). La croissance optimale et le développement rapide des plantes des 4 variétés ont été observés sur le milieu contenant IAA+K+GA3.
Des pousses multiples se sont formées sur les milieux contenant des concentrations élevées en GA3 (5 et 10 μM), notamment sur les variétés Cira et Blanik (fig. 3). Les plantes obtenues à partir de culture de méristèmes apicaux ont pû être continuellement propagées en conditions stériles dans de la perlite saturée d'une solution de Hoagland avec addition de 0,1 μM de IAA. Les plantes se développent à partir des bourgeons axillaires; une plantule d'origine méristématique est capable de donner naissance à 5 à 8 plantes en 2 mois. L'article décrit le système de formation des pousses multiples et la propagation continue in vitro pour la maintenance et la multiplication de variétés de pommes de terre indemnes de maladies (Westcott et al., 1977) et de virus (fig. 4).
Article PDF
Similar content being viewed by others
Avoid common mistakes on your manuscript.
References
Chromova, L. M., L. N. Trofimec & V. A. Knjazev, 1977. The influence of growth regulators on morphogenesis of cultured apical meristem.Nauchnye Trudy Nikch (Kiev) 30: 19–25 (in Russian).
Denton, I. R., R. J. Westcott & B. V. Ford-Lloyd, 1977. Phenotypic variation ofSolanum tuberosum L. cv. Dr Mc Intosh regenerated directly from shoot-tip culture.Potato Res. 20: 131–136.
Gamborg, O. L., R. A. Miller & K. Ojima, 1968. Nutrient requirements of suspension cultures of soybean root cells.Exp. Cell Res. 50: 151–158.
Gamborg, O. L. & L. R. Wetter (Eds.), 1975. Plant tissue culture methods. National Research Council of Canada, Praire Regional Laboratory, Saskatoon, Saskatchevan, Canada, 109 pp.
Gregorini, G. & R. Lorenzi, 1974. Meristem-tip culture of potato plants as a method of improving productivity.Potato Res. 17: 24–33.
Henshaw, G. G., R. J. Westcott & W. M. Roca, 1978. Tissue culture methods for the storage and utilization of potato germplasm. 4th International Congress of on Plant Tissue and Cell Culture, (1978), University of Calgary, Canada. Abstract No 1204.
Hussey, G., 1976. In vitro release of axillary shoots from apical dominance in monocotyledons plantlets.Ann. Bot. 40: 1323–1326.
Ingram, D. S., 1973. Growth of plant parasites in tissue culture. In: H. E. Street (Ed.), Plant tissue and cell culture, Blackwell, Oxford, pp. 392–421.
Kartha, K. K., S. Champoux, O. L. Gamborg & K. Pahl, 1977. In vitro propagation of tomato by shoot apical meristem culture.J. Am. Soc. hort. Sci. 102: 346–349.
Lam, S. L., 1975. Shoot formation in potato tuber dise in tissue culture.Am. Potato J. 52: 103–106.
Mellor, F. C. & R. Stace-Smith, 1977. Virus-free potatoes by tissue culture. In: J. Reinert & Y. P. S. Bajaj (Eds.), Applied and fundamental aspects of plant cell, tissue, and organ culture. Springer Verlag, Berlin-Heidelberg-New York, pp. 616–635.
Morel, G., 1975. Meristem culture techniques for the long-term storage of cultivated plants. In: O. Frankel & J. G. Hawkes (Eds.), Crop genetic resources for today and tomorrow. University Press, Cambridge, pp. 327–332.
Morel, G. & C. Martin, 1955. Guérison de pommes de terre atteintices de maladies a virus.C. r. Acad. Sci., Paris 41: 472–474.
Murashige, T. & F. Skoog, 1962. A revised medium for rapid growth and bioassays with tobacco tissue cultures.Physiologia Pl. 15: 473–497.
Novák, F. J. and I. Maŝková, 1979. Apical shoot tip culture of tomato.Scientia Hort. 10: 337–344.
Pennazio, S. & P. Redolfi, 1973. Factors affecting the culture in vitro of potato meristem tips.Potato Res. 16: 20–29.
Petrů, E., 1976. Docílení viruprosté sadby metodou meristémových kultur. In: J. Zadina & E. Jermoljev (Eds.), Ŝlechtení bramboru. Academia, Praha, pp. 327–332.
Quak, F., 1961. Heat treatment and substances inhibiting virus multiplication in meristem culture to obtain virus-free plants.Adv. Hort. Sci. Appl. 1: 144–148.
Simon, P. W. & S. J. Péloquin, 1977. The influence of parental species on the origin of callus in another culture ofSolanum hybrids.Theor. appl. Genet. 50: 53–56.
Svobodová, J., 1966. Elimination of viruses by means of callus tissue culture. In: A. B. R. Beenstra & J. Dykstra (Eds.), Virus in plants. John Wiley, New York-London, pp. 48–53.
Wang, P. J., 1977. Regeneration of virus-free potato from tissue culture. In: W. Barz, E. Reinhard & M. H. Zenk (Eds.), Plant tissue culture and its bio-technological application. Springer Verlag, Berlin-Heidelberg-New York, pp. 386–391.
Wang, P. J., 1978. Gene preservation and foundation stock seed production of potato in vitro. 4th International Congress on Plant Tissue and Cell Culture (1978), University of Calgary, Canada. Abstract No 1205.
Westcott, R. J., G. G. Henshaw & W. M. Roca, 1977. Tissue culture storage of potato germplasm: Culture initiation and plant regeneration.Pl. Sci. Lett. 9: 309–315.
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Novák, F.J., Zadina, J., Horáĉková, V. et al. The effect of growth regulators on meristem tip development and in vitro multiplication ofSolanum tuberosum L. plants. Potato Res 23, 155–166 (1980). https://doi.org/10.1007/BF02356266
Accepted:
Published:
Issue Date:
DOI: https://doi.org/10.1007/BF02356266