Abstract
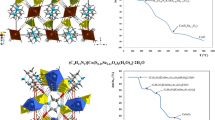
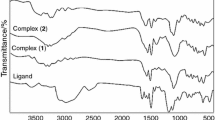
BaSeO3·2·5H2O(I), PbSeO3· 2H2O(II) and CdSeO3·3.5H2O(III) were prepared and analysed. Their hygroscopicity and solubility was investigated. These compounds have high thermal Stability, as shown by their TG and DTA data. IR spectra show multi-dentate coordination of selenite to cations, due to considerable splitting of the asymmetric v3 and v4 bands of SeO 23 − in the 780-730 cm−1 and 420-325 cm−1 region.
Tentative structures have been proposed involving bridging oxygen atoms.
Zusammenfassung
BaSeO3-2.5H2O(I), PbSeO3 · 2H2O(II) und CdSeO3· 3.5H2O(III) wurden hergestellt, analysiert sowie deren Hygroskopizität und Löslichkeit untersucht. TG- und DTA-Untersuchungen erweisen die hohe thermische Stabilität dieser Verbindungen. Die IR-Spektren zeigen mehrzählige Koordination von Selenit zu Kationen, was aus einer beträchtlichen Aufspaltung der antisymmetrischenv 3 undv 4 Banden von SeO 23 − im Bereich 780-730cm−1 bzw. 420-325 cm−1 hervorgeht. Es wurden versuchsweise Strukturen mit überbrückenden Sauerstoffatomen vorgeschlagen.
Резюме
Вновь полученные сое динения BaSeO3· 2,5H2O, PbSeO3 · 2H2O и CdSeO3 · 3,5H2O охарактеризованы эл ементным анализом и и зучена их гидроскопйчность и р астворимость. Согласно данным ТГ и Д ТА соединения облада ют высокой термоустойчивостью. ИК спектры показали полидентат ную координацию селе нит-аниона по отношению к катионам, вызывая значительное расщеп ление симметричныхv 3 иv 4 полос SeO 23 }- в области 780-730 и 420-325 см−1. Для всех соединений п редложены пробные ст руктуры, включающие мостиков ые атомы кислорода.
Article PDF
Similar content being viewed by others
Explore related subjects
Discover the latest articles, news and stories from top researchers in related subjects.Avoid common mistakes on your manuscript.
References
V. P. Verma, Ph.D. Thesis (1974) I.I.T. New Delhi, India.
M. Qureshi, R. Kumar and V. Sharma, Anal. Chem., 46 (1974) 1855.
J. P. Rawat, M. A. Khan and Pritam Singh, Bull. Chem. Soc. (Japan), 57 (1984) 1701.
M. Ebert and D. Havelicek, Coll. Czech. Chem. Commun., 46 (1981) 1740.
A. I. Vogel, A Textbook of Quantitative Inorganic Analysis including Elementary Instrumental Analysis, 1978, pp. 452, 457 and 467 Longman, 4th Edn.
K. Sathianandan, L. D. McCory and J. L. Margrave, Spectrochim. Acta, 20 (1964) 957.
T. Losoi and J. Valkonen, Finn. Chem. Lett., 1 (1984) 1.
Mellor's Modern Inorganic Chemistry, revised and edited by G. D. Parkes, Longmans Green and Co., London (1963).
W. D. Harrison, J. B. Gill and D. C. Goodall, Polyhedron, 2 (1983) 153.
H. D. Lutz, S. M. El. Suradi and B. Englen, Z. Naturforsch., Teil B, 32 (1977) 1230.
B. L. Khandelwal and V. P. Verma, J. Inorg. Nucl. Chem., 38 (1976) 763.
F. A. Cotton and R. Francis, J. Am. Chem. Soc., 82 (1960) 2986.
W. Stuart and T. L. Whatley, J. Inorg. Nucl. Chem., 31 (1969) 1639.
M. Vedali, P. A. Vigate, G. Bandoli, D. A. Clements and V. Casellato, Inorg. Chem. Acta, 6 (1972) 671.
Author information
Authors and Affiliations
Rights and permissions
About this article
Cite this article
Verma, V.P., Khushu, A. Thermal and other studies on bivalent metal selenltes. Journal of Thermal Analysis 35, 1157–1163 (1989). https://doi.org/10.1007/BF01913033
Issue Date:
DOI: https://doi.org/10.1007/BF01913033