Abstract
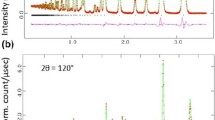
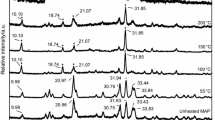
The oxidative behaviour of natural pentlandite (FeNi)9S8 has been studied by thermogravimetry (TG) and differential thermal analysis (DTA) in a dynamic oxygen atmosphere (0.21 min−1) over the temperature range 20–1000°. Gaseous products were analysed by a coupled quadrupole mass spectrometer. The reaction products at various intermediate temperatures were characterised by X-ray diffractometry and chemical analysis. A reaction sequence has been deduced, in which in the temperature range 460–700° pentlandite breaks down with the formation of Fe2O3, NiSO4, NiO, NiS and NiFe2O4; FeSO4 was also formed but decomposed above 640°. Beyond 700° NiS was completely oxidised, and NiSO4 decomposed slowly. Another sulphide phase, possibly Ni3±xS2, was formed at 740° and completely oxidised at 790°, and above 800° NiSO4 decomposed completely leaving only Fe2O3, NiO and NiFe2O4 as stable products.
Résumé
On a étudié, par thermogravimétrie (TG) et par analyse thermique différentielle (ATD), en atmosphère dynamique d'oxygène (0.21 min−1) et dans l'intervalle de températures allant de 20 à 1000°, le comportement de la pentlandite (FeNi)9S8 vis-à-vis de l'oxydation. On a analysé les produits gazeux formés avec un spectromètre de masse quadrupole couplé. On a caractérisé les produits de réaction à diverses températures intermédiaires par diffractométrie des rayons X et par analyse chimique. On en a déduit une séquence de réaction, dans laquelle la pentlandite se décompose dans l'intervalle 450–700° avec formation de Fe2O3, NiSO4, NiO, NiS et NiFe2O4; FeSO4 se forme également, mais se décompose au-dessus de 640°. Au-dessus de 700° NiS est complètement oxydé, et NiSO4 se décompose lentement. Une autre phase sulfurée, probablement Ni3±xS2 se forme à 740° et est oxydée complètement à 790°. Au-dessus de 800°, NiSO4 se décompose completèment ne laissant que Fe2O3, NiO et NiFe2O4 comme produits stables.
Zusammenfassung
Das oxidative Verhalten von natürlichem Pentlandit (FeNi)9S8 wurde durch Thermogravimetrie (TG) und Differentialthermoanalyse (DTA) in einer dynamischen Sauerstoffatmosphäre (0.21 min−1) im Temperaturbereich 20–1000° untersucht. Die gasförmigen Produkte wurden durch ein gekoppeltes vierpoliges Massenspektrometer analysiert. Die Reaktionsprodukte bei verschiedenen Zwischentemperaturen wurden durch Röntgen-diffraktometrie und chemische Analyse charakterisiert. Es wurde eine Reaktionssequenz abgeleitet, bei welcher Pentlandit im Temperaturbereich von 450 bis 700° unter Bildung von Fe2O3, NiSO4, NiO, NiS und NiFe2O4 zersetzt wird; FeSO4 wurde auch gebildet, wurde aber bei Temperaturen über 640° zersetzt. Über 700° wurde NiS vollständig oxidiert und NiSO4 langsam zersetzt. Eine weitere Sulfidphase, möglicherweise Ni3±xS2 wurde bei 740° gebildet und bei 790° vollständig oxidiert. Über 800° wurde NiSO4 vollständig zersetzt, wobei nur Fe2O3, NiO und NiFe2O4 als stabile Produkte zurückblieben.
Резюме
Было изучено окислит ельное поведение природного пентланд ита (FeNi)9S8 с помощью термограви метрии и дифференциа льного термического анализ а в динамической атмосфере кислорода (0.2 1 мин−1) в области темпе ратур 20–1000°. Газообразные продукты анализиров ались квадрупольным масс-спектрометром. П родукты реакции при промежуточных темпе ратурах были охаракт еризованы рентгеновской дифра ктометрией и химическим анализом. Выведена последоват ельность реакций. В области тем ператур 450–700° пенталандит расщ епляется с образован ием Fe2O3, NiSO4 NiO, NiS и NiFe2O4. При этом также образу ется FeSO4, разлагающийся выше 640°. NiS выше 700° полностью окисляется, и NiSO4 — медле нно разлагается. Друг ая сульфидная фаза, возм ожно состава Ni3±xS2, образуется при 740° и полностью разлагает ся при 790°. Выше 800° полностью разлагается NiSO4 и остаю тся в качестве стабил ьных веществ только Fe2O3, NiO и NiFe2O4.
Article PDF
Similar content being viewed by others
Explore related subjects
Discover the latest articles, news and stories from top researchers in related subjects.Avoid common mistakes on your manuscript.
References
T. Kennedy andB. T. Sturman, J. Thermal Anal., 8 (1975) 329.
J. G. Dunn andC. E. Kelly, J. Thermal Anal., 12 (1977), 43.
G. Kullerud, Carnegie Inst. Wash. Year Book, 62 (1962) 174.
A. J. Naldrett, J. R. Craig andG. Kullerud, Econ. Geol., 62 (1967) 826.
K. C. Misra andM. E. Fleet, Econ. Geol., 68 (1973) 518.
A. V. Vanyukov, Chem. Abstr., 84 (1976) 63030 q.
T. R. Ingraham andP. Mauriar, Trans. Met. Soc. AIME, 242 (1968) 2039.
P. G. Thornhill andL. M. Pidgeon, J. Metals, 9 (1957) 989.
W. E. Ewers, Proc. Australasian Inst. Min. Met., 241 (1972) 19.
G. Kullerud andR. A. Yund, J. Petrol., 3 (1962) 126.
G. Kullerud, Carnegie Inst. Wash. Year Book, 58 (1958) 161.
T.Kennedy and I. W.Twaddle, ANZ 3rd conf. Mass. Spect. Canberra, 1975.
G. Kullerud, Can. Mineral., 7 (1963) 353.
A. P. Likhachev andY. A. Brauer, Dokl. Akad. Nauk. USSR, 186 (1969) 154.
Author information
Authors and Affiliations
Additional information
We wish to thank Dr. W. Barker (CSIRO) for the sample of pentlandite and valuable information, Dr. B. O'Conner (Physics) for XRD work, and Messrs. K. Oliver, B. Sturman and I. Twaddle (Chemistry) for technical assistance.
Rights and permissions
About this article
Cite this article
Dunn, J.G., Kelly, C.E. A TG/MS and DTA study of the oxidation of pentlandite. Journal of Thermal Analysis 18, 147–154 (1980). https://doi.org/10.1007/BF01909462
Received:
Issue Date:
DOI: https://doi.org/10.1007/BF01909462